Bir çözelti, iki veya daha fazla maddeden oluşan homojen bir karışım iken, çözünürlük, bir dizi çözücü içinde çözünebilen bir bileşik veya maddenin maksimum miktarıdır .
Günlük yaşamda karşılaştığımız çeşitli çözümlerin çoğu bir bardak tatlı şurup içerir. Bir bardak şurupta su, şurup ve şeker olmak üzere birkaç bileşen vardır.
Bu bileşenler, bileşen bileşenler artık görünmeyene kadar karıştırılırsa, o zaman bir çözüm haline gelir.
Çözümü tartışırken, aşağıdaki ileri inceleme, çözümün tanımını, özelliklerini, türlerini ve faktörlerini içerir.
Çözelti ve çözünürlüğün tanımı

Çözüm
Çözelti, iki veya daha fazla maddeden oluşan homojen bir karışımdır. Çözümü oluşturan bileşenler nedeniyle çözüm olarak adlandırıldı.
Bir çözümde çözücüler ve çözücüler vardır. Çözünen (çözünen), bir çözeltide daha az miktarda bulunan bir çözelti oluşturan bir maddedir. Bu arada çözücü (çözücü), çözünen maddeden daha bol bulunan bir maddedir.
Çözeltideki deniz maddesinin bileşimi, çözeltinin konsantrasyonu ile ifade edilir. Bir çözelti oluşturmak için bir çözücü ve bir çözücünün karıştırılması işlemine çözme veya çözme denir.
Çözüm hakkında daha fazla bilgi edinmek için aşağıdaki resim görüntüsünü inceleyin.
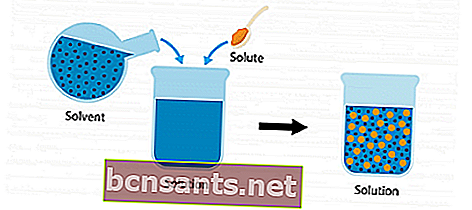
Bir çözünen ve bir çözücü var. İki bileşen bir kapta karıştırılıp birleştirildiğinde, bir çözelti haline gelir.
Çözünürlük (ler)
Çözünürlüğün anlamı, bir dizi çözücü içinde çözünebilen bir bileşik veya maddenin maksimum miktarıdır.
Çözünürlük, mol / L birimlerinde s (solibility) ile sembolize edilir veya yaygın olarak molarite birimleri M kullanır. Çözünürlük veya molarite için formül.
M = n / V
M, molarite (mol / L), n, maddenin mol sayısıdır (mol) ve V, çözelti veya çözücünün hacmidir (L).
Çözünürlük, belirli bir miktarda çözücü içinde hala çözünebilen bir maddenin konsantrasyonu olarak da tanımlanır.
Sabit Çözünürlük Ürünü (Ksp)
Bir çözücü içinde çözünen bir çözünen, bir denge reaksiyonu oluşturacaktır. Dengenin oluşması, çözünmeyen çözünen maddeler ve çözünen iyonlardan etkilenir.
Ayrıca şunu okuyun: 100'den Fazla Standart ve Standart Olmayan Kelime + Açıklama [GÜNCELLENMİŞ]Aşağıdaki, bir reaksiyon için denge sabitinin bir örneğidir.
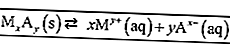
Denge formülünü yazma kurallarına göre, formüle sadece çözelti (aq) ve gaz (lar) şeklindeki maddeler yazılır. Böylece elde edilir:
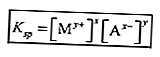
Çözülmesi zor bir çözelti için denge sabiti, çözünürlük ürün sabiti (Ksp) olarak adlandırılır.
Çözüm Özellikleri

Çözümde ortaya çıkan fiziksel özellikler üçe ayrılır:
1. Çözümlerin Kolligatif Özellikleri
Bir solüsyondaki çözünen partikül sayısına bağlı olan ve solvent partiküllerinin tipine bağlı olmayan bir solüsyon özelliğidir.
Kolligatif özellikler, bileşenlerin türüne veya kimyasal özelliklerine bakılmaksızın çözelti içindeki çeşitli elektrolit olmayan maddelerin konsantrasyonuna eşdeğerdir.
Bir sıvı içindeki katıların bir solüsyonunun kolligatif özelliklerinin belirlenmesinde, katının uçucu olmadığı kabul edilir ve solüsyonun üzerindeki buhar basıncı tamamen solventten gelir.
Bir çözeltinin kolligatif özelliklerinden bazıları ozmotik basınç, buhar basıncında azalma, kaynama noktasında artış ve donma noktasında azalmadır.
2. Katkı özellikleri
Çözeltide, katkı özellikleri, moleküldeki toplam atomlara veya çözeltinin kurucu özelliklerinin sayısına bağlı olan bir çözeltinin özellikleridir.
Çözeltilerin katkı özelliklerine bir örnek, atomik kütlelerin toplamı olan moleküler ağırlıktır.
Bir çözeltinin bileşenlerinin kütlesi, katkı özelliklerine dahil edilir, çözeltinin toplam kütlesi, çözeltinin her bir bileşeninin, yani çözünen ve çözücü miktarıdır.
3. Yapısal Doğa
Bu, molekülün atomlarına (atom türüne ve atom sayısına) bağlı olan çözeltinin doğasını içerir. Yapısal özellikleri, sistemdeki tek bileşiklerin ve molekül gruplarının kurallarını gösterir.
Kısmen eklemeli ve yapıcı olan birkaç fiziksel özellik vardır. Bunların arasında bazı yapısal ve bazı katkı maddelerinde yer alan ışık kırılması, elektriksel özellikler, yüzey ve yüzeyler arası özellikler vardır.
Çözüm Türü

1. Doymamış Çözüm
Doymamış çözelti, doymuş bir çözelti yapmak için gerekenden daha az çözünen içeren bir çözelti olarak tanımlanır. Doymamış çözeltiler, madde ile doğru şekilde reaksiyona girmemiş partiküller içerir, yani maddeyi yine de çözebilirler.
İyon konsantrasyon değeri <Ksp. Olduğunda çözeltinin doymamış olduğu söylenir. Doymamış bir çözelti içinde çözünen çökelme yoktur.
Ayrıca şunu okuyun: Kimyasal çözeltilerin tanımı, türleri ve bileşenleri2. Doymuş Çözüm
Çözünen madde ve çözücü arasında bir denge olduğunda doymuş bir çözelti içine bir çözelti dahil edilir. Doymuş bir solüsyonda partiküller reaktifle tam olarak reaksiyona girer veya maksimum konsantrasyon yaşarlar.
İyon konsantrasyonu Ksp değeri ile aynıysa çözeltinin doymuş olduğu söylenir. Bu denge koşulunda, çözücü içindeki çözünen maddenin hızı, çökelme hızı ile aynıdır. Yani çözeltideki maddenin konsantrasyonu aynıdır.
3. Yüksek Doymuş Çözüm
Bu çözücüden daha fazla çözünen içeren bir çözümdür. Bu, iyon konsantrasyonunun ürün değerinin> Ksp'ye neden olur, böylece çözelti doyurulur ve çöker.
Çözünürlük Faktörü

Bir sıvının çözünürlüğü değişir. Bu, birkaç çözünürlük faktöründen etkilenir. İşte çözünürlük faktörlerinden bazıları.
1. Sıcaklık
Çözeltinin sıcaklık seviyesi, çözünen çözülme sürecini etkiler. Daha yüksek sıcaklıklarda, çözünen, çözücü içinde kolaylıkla çözünecektir.
Bunun nedeni, daha yüksek sıcaklıklardaki katı parçacıkların daha hızlı hareket ederek daha sık ve etkili çarpışmalara izin vermesidir.
2. Çözünen maddenin boyutu
Çözünen granüller ne kadar küçükse, çözücü içinde o kadar kolay çözülür. Az miktarda çözünen granül, maddenin yüzey alanının daha geniş olmasına ve bir çözelti içinde yayılmasına neden olur.
Maddenin yüzey alanı ne kadar büyükse, o kadar çok parçacık birbiriyle çarpışır. Çözülme sürecinin daha hızlı gerçekleşmesine neden olan şey budur.
3. Çözücü hacmi
Çözücünün büyük hacmi, maddenin çözülme sürecini etkiler. Bunun nedeni, çözücü partiküllerinin giderek daha fazla çözünen madde ile reaksiyona girmesidir.
Kullanılan çözücü hacmi ne kadar fazlaysa, çözünen çözme işlemi o kadar hızlı olacaktır.
4. Karıştırma hızı
Karıştırma faktörünü eklerseniz çözme işlemi daha hızlı olacaktır.
Karıştırılarak, çözünen parçacıklar çözücü ile giderek daha fazla karıştırılır, böylece çözme reaksiyonu, karıştırmadan çözülmekten daha hızlı olur.
Bu, anlamı, özellikleri, türleri ve faktörleri ile birlikte çözüm ve çözünürlüğün bir açıklamasıdır. Faydalı olabilir.
